دانستنی های باطری
تعریف باترى
به طور ساده میتوان باتری را یک سلول تعریف کرد که میتواند انرژی شیمیایی را به به انرژی الکتریکی تبدیل کند. یک باتری با انجام واکنشهایی شیمیایی درون خود، انرژی شیمیایی موجود را به انرزی الكتریكی تبدیل می كند. باترى بسته به مشخصات ساختاری و نوع استفاده از آن، میتواند عمری بین چند ساعت تا چند هفته داشته باشد.
باتری های مختلف دارای مواد و واکنش های شیمیایی متفاوتی هستند بنابراین در تقسیم بندی کلی در دو دسته غیر قابل شارؤ (باتری های اولیه) و قابل شارژ (باتری های ثانویه) تعریف می شوند. باتریهای اولیه یکبار استفاده شده و دور انداخته میشوند، زیرا ترکیب شیمیایی مواد الکترود در هنگام تخلیه بر گشتناپذیر، دچار تغییر میشوند. یک نمونه معمول باتری اولیه روی-کربن است که می توانند در چراغ قوه ها، ساعتهای دیواری، کنترلهای لوام صوتی و تصویری و دیگر دستگاه های قابل حمل استفاده شوند.
باتریهای ثانویه (قابل شارژ) با استفاده از جریان الکتریکی اعمال شده میتوانند چندین بار تخلیه و شارژ شوند. ترکیب شیمیایی اصلی الکترودها را میتوان با جریان الکتریکی معکوس، بازیابی کرد. به عنوان مثال میتوان به باتریهای اسید-سرب که در وسایل نقلیە استفادە میشوند و باتریهای لیتیوم-یون كه براى تجهيزات الكترونيكى قابل حمل مانند لب تاپها وتلفن هاى همراه استفاده میشود، اشاره کرد.
ساختار باترى
قسمت اصلی یک باتری که انرژی الکتریکی لازم را فراهم می کند، سلول (Cell) نام دارد. سلول باتری از ٣ جزء (دو الکترود و یک ماده شیمیایی به نام الكتروليت) تشكیل شده است. جهت ايزوله كردن سلول از محيط بيرون وهمچنين فراهم كردن ايمنى و راحتی استفاده، سلول درون یک بسته (فلز یا پلاستیکی) قرار دارد. در این بسته خارجی دو الکترود با علامتهای + (قطب مثبت) و – (قطب منفی) وجود دارد که به دو الکترود داخلی سلول متصل هستند.
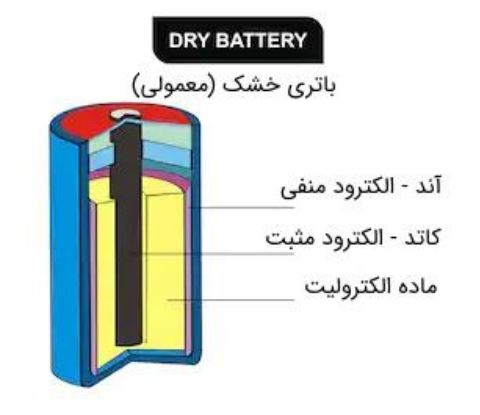
عملکرد باترى
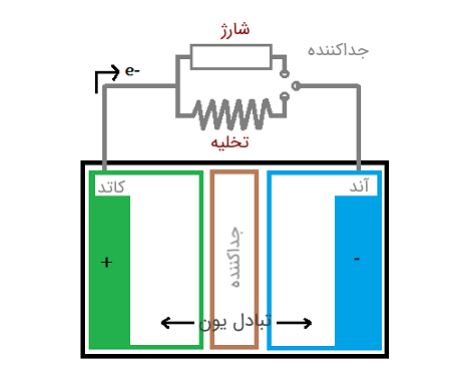
هر باتری بر اساس یک واکنش شیمیایی، یعنی واكنش اكسایش-كاهش كار مى كند. اين واكنش بين كاتد وآند واز طريق الكتروليت رخ میدهد. در نتیجه، یک الکترود به علت واکنش اکسایش به صورت منفی باردار میشود. این الکترود، کاتد نام دارد. الکترود دیگربه علت واکنش کاهش به صورت مثبت باردار میشود که آن را آند مینامند. هنگامی که دو نوع فلز مختلف در محلول الکترولیت یکسانی فرو برده شوند، یکی از الکترودها الکترون میگیرد و دیگری الکترون از دست میدهد.
در نتیجه، یکی از فلزها الکترون میگیرد و دیگری الکترون از دست خواهد داد. این اختلاف در تراکم الکترون دو فلز، بین فلزها اختلاف پتانسیل الکتریکی ایجاد میکند. این اختلاف پتانسیل می تواند به عنوان منبع ولتاز در هر وسیله الکتریکی استفاده شود. یونها فقط از طریق جداکننده جریان مییابند و جداكننده تمام حرکات از آند به كاتد را مسدود می کند. بنابراین، تنها راه دریافت جریان خارجی، از طریق پایانههای باترى است.
هر باتری یک مقاومت داخلی (R) دارد و اختلاف پتانسیل بین قطبهای باتری (V)، زمانی که جریان (I) از آن می گذرد، برابر V=Eemr – IR میباشد. فرایند تبدیل انرزى در باترى باعث افزايش مقاومت الكتريكى داخلى آن مى شود واين حالت تا آنجا پيش میرود که نیروی محر که (Eemf) دیگر توانایی غلبه بر آن را ندارد. افزایش مقاومت الکتریکی در باتری به دلیل نفوذ ماده كاتد به داخل ماده آند رخ میدهد. در برخی از مواقع میتوان با گرم و سرد کردن باتری (انداختن در آب جوش و منقبض و منبسط كردن باتری) یا زدن ضربه، مسیرهای جدیدی را برای عبور جریان ایجا کرده و مقاومت R را تا حدودی کم کرد.
به محض اینکه باتری به مدار خارجی متصل شود، یک جریان در باتری و همچنین مدار جاری می شود. در اثر این جریان در باتری، یک افت ولتاژ درون باتری اتفاق می افتد که بعلت مقاومت داخلی خود باتری است. پس وقتی مدار خارجی متصل می شود، ولتازظاهر شده در قطب باتری چیزی کمتر از ولتاژ مدار باز باطری است. این بدلیل افت ولتاز در اثر مقاومت درونی باتری است. در واقع، اختلاف EMF نسبت به افت ولتاژ داخلی در طول قطب های باتری است که در زمان اتصال مدار خارجی به آن ظاهر می شود.
ظرفیت باترى
انرژی ذخیره شده در باتری ظرفیت باتری نامیده می شود و با جرم فعال ماده تعیین می شود. ظرفیت باتری حداکثر میزان انرزیرا ارائه می دهد که می تواند از باتری تحت شرايط مشخص معينی استخراج شود. ظرفيت های واقعی ذخيره انرزى باترى مى تواند به طور معنی داری از ظرفیت صوری آن متفاوت باشد. ظرفیت باتری به شدت به عمر باتری، نوع ماده فعال، شارز شدن یا تخلیه شدن باترى ودما بستكى دارد. ظرفيت باترى با وات ساعت (Wh)، كيلووات- ساعت (kWh) يا آمپر ساعت (Ah) اندازه كيرى مىشود. متداول ترين واحد ظرفيت باترى Ah است. ظرفيت باترى هاى قلمى ونيم قلمى معمولا با واحد ميلى آمير ساعت (mAh) نشان داده می شود. یعنی یک باترى ٢٠٠٠ ميلی آمپر ساعت به مدت ١ ساعت جریانى به شدت ٢٠٠٠ ميلی آمپر یا به مدت ١٠٠ساعت جريان ٢٠ ميلى آمپر فراهم مى كند.